99Mo zerfällt mit einer Halbwertszeit von
66,02 Stunden in das metastabile
99mTc. Dabei
wandelt sich ein Neutron unter Herausschleudern eines
Elektrons in ein Proton um, so dass die Kernladungszahl Z um 1
ansteigt, die Massenzahl aber gleich bleibt. Aus Molybdän
(Z = 42) wird also Technetium (Z = 43).
99Mo → 99mTc + e–
(Kernreaktion im Generator)
Der metastabile
99mTc-Kern muss noch Energie abgeben.
Er zerfällt mit einer Halbwertszeit von 6,02 Stunden unter
Aussendung von
γ-Strahlung
in
99Tc.
99mTc → 99Tc + γ-Strahlung
(Für die Szintigraphie maßgebende Kernreaktion)

|

|
Generator zur Erzeugung von 99mTc aus 99Mo.
|
|
Generator zur Erzeugung von 99mTc aus 99Mo.
|
Das Prinzip des Molybdän-99/Technetium-99m-Generators wurde um 1960 am Brookhaven
National Laboratory (USA) entwickelt. Der Generator besteht aus einer
chromatografischen Säule 1 ,
die mit Aluminiumoxid gefüllt ist. Am Aluminiumoxid haftet das aus Kernreaktoren
gewonnene Uran-Spaltprodukt
99Mo. Um die Strahlenbelastung für Transport
und Bedienung möglichst gering zu halten, ist die Säule mit dicken
Bleiwänden 2 gekapselt.
Während das Mutternuklid
99Mo als Molybdat (MoO
42–)
fest am Aluminiumoxid-Trägermaterial der Säule haftet, kann das entstehende
Pertechnetat (TcO
4– ) leicht herausgelöst werden. Die
Säule 1 ist
unten mit einem
Vorratsbehälter 3
verbunden, der physiologische Kochsalzlösung enthält. Um das gebildete
99mTc
herauszulösen, wird auf die
obere Kanüle 5
das
Elutionsgefäß 4 ,
ein Glasfläschchen mit durchstechbaren Propfen, aufgesetzt. Im Glasfläschchen
herrscht ein Vakuum. In Folge des Unterdrucks im Elutionsgefäß wird physiologische
Kochsalzlösung aus dem
Behälter unten 3
über die
chromatografische Säule 1
angesaugt. Beim Durchströmen der Säule wird das aus Molybdän entstandene
99mTc als Natriumpertechnetat aufgenommen.
Die Natriumpertechnetatlösung steht nun zur Injektion am Patienten, z.B. bei
Schilddrüsenuntersuchungen, zur Verfügung. Zur Aufnahme von Szintigrammen
anderer Organe werden spezielle Substanzen, die vom Körper in die entsprechenden
Organe transportiert werden, mit dem Pertechnetat radioaktiv markiert.
Die 99m-Tc-Natriumpertechnetat-Lösung im
Elutionsgefäß 4
wird mit einem speziellen Greifwerkzeug 6
aus dem Strahlenschutzbehälter 7
herausgenommen (rechtes Bild). Der Strahlenschutzbehälter besteht aus Wolfram. Zur
Sichtkontrolle ist er mit einem Bleiglasfenster 8
versehen.
|
|
|
Mit Strahlenwarnzeichen gekennzeichnete Pertechnetat-Lösung 4 .
|

Mit Strahlenwarnzeichen gekennzeichnete Pertechnetat-Lösung 4 .
|
|

|
|
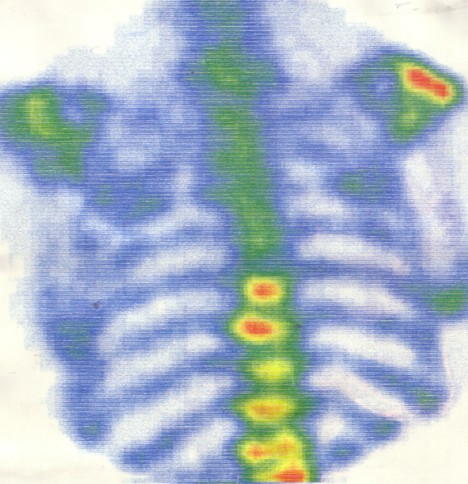
Die mit 99mTc markierte Lösung für Skelettuntersuchungen wird
dem Patienten injiziert. Sie lagert sich speziell in Bereichen veränderten
Knochenwachstums an. Mit Hilfe von Detektoren lässt sich die
γ-Strahlung außerhalb des Körpers
registrieren. Computerprogramme erstellen aus den Messwerten ein Bild des Skeletts.
Das oben abgebildete Szintigramm zeigt Krebsmetastasen im Bereich des
Schultergelenks und der Wirbelsäule.
|




