1787 wurde von dem Amateurgeologen Leutnant
Carl Axel Arrhenius
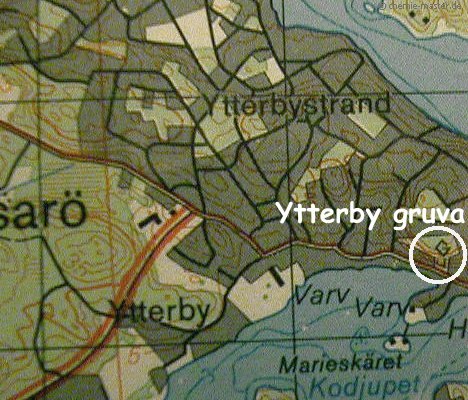
in der »Ytterby gruva« ein schwarzes, schweres, bisher
unbekanntes Mineral gefunden. Dieses Mineral nannte man zunächst
Ytterbit. Bei einer für die damalige Zeit sehr komplizierten
Analyse fand
Johan Gadolin von der Universität Abo 1794
heraus, dass Ytterbit zu 38% aus einer bisher unbekannten »Erde«
besteht. Die Oxide der Metalle nannte man damals »Erden«.
Die neu entdeckte Erde erhielt den Namen »Yttererde«. Mit
ihrer Entdeckung war die Tür zur
Entdeckung der »Seltenen Erden«
aufgestoßen. Das Mineral Ytterbit wurde 1800 zu Ehren Gadolins
in Gadolinit umbenannt.
Carl Gustav Mosander, Professor in Stockholm, untersuchte 1843
die »Yttererde« genauer und entdeckte dabei, dass diese
neben Yttriumoxid noch andere bisher unbekannte Oxide
(
Terbiumoxid und
Erbiumoxid)
enthielt. Unreines Yttrium hatte
Friedrich Wöhler bereits
1824 durch Reduktion von Yttriumchlorid mit Kalium erhalten. Reines
Yttrium-Metall wurde erstmals 1935 hergestellt (
West und
Hopkins).

|

|
Gadolinit (schwarz) aus der Ytterby gruva.
(Mineraliensammlung der Bergskola Falun, Stora Museum Bergwerk Falun)
|
|
(Mineraliensammlung der Bergskola Falun, Stora Museum Bergwerk Falun)
Gadolinit (schwarz) aus der Ytterby gruva.
|