
chemie-master.de
Website für den Chemieunterricht
 |
chemie-master.de |
Website für den Chemieunterricht |
Metall
Übergangsmetall
VI. Nebengruppe
[Rn]5f146d47s2

|
|
Glenn T. Seaborg (1912-1999, Mitentdecker von Plutonium, Americium, Curium, Berkelium, Californium, Einsteinium, Fermium, Mendelevium und Nobelium) zeigt auf das Element Seaborgium im Periodensystem. Er ist der einzige Wissenschaftler, nach dem zu seinen Lebzeiten ein chemisches Element benannt wurde. |
|
|
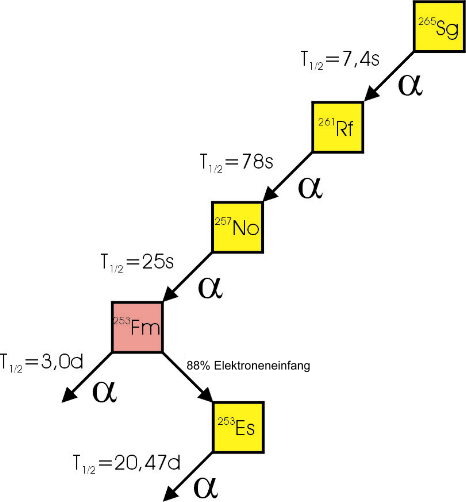
Quelle: Dr. Kronenberg, Los Alamos National Laboratory, USA Zerfallskette von 265Sg. |
Information: Dr. A. Kronenberg
 |
Nur Radionuklide, keine stabilen Isotope. |